Теория егэ по химии
Содержание:
- Важные даты
- Как выбрать учебник по химии
- Теория к заданию 11 из ЕГЭ по химии
- Какой учебник по химии лучше
- Пример 1
- Какие темы есть в ЕГЭ по химии?
- Пример 2
- Сдавать ли химию в 2021 году?
- Бесплатно
- Общая информация
- Виртуальные лаборатории
- Теория к заданию 10 из ЕГЭ по химии
- Что такое равновесие?
- Рейтинг учебников по химии
Важные даты
Важно! Досрочной сдачи ЕГЭ в 2021 году не будет! Весенняя сессия отменена из-за высоких показателей заболеваемости COVID-19. Согласно календарю ЕГЭ 2021 года экзамен по химии выпускники будут сдавать в первый день основного периода
Согласно календарю ЕГЭ 2021 года экзамен по химии выпускники будут сдавать в первый день основного периода.
| Основной период | |
| Основной день | 24 мая 2021 года |
| Резерв |
29 июня 2021 года 1 июля 2021 года |
Также смотрите основные даты других предметов ЕГЭ в календаре основной сессии 2021 года.
Важно! Для пересдачи данной дисциплины определены резервные дни. Пересдать ЕГЭ по химии осенью 2021 года будет нельзя, так как в рамках сентябрьской сессии предполагается пересдача только обязательных предметов
Как выбрать учебник по химии
Определитесь с целью обучения и уровнем знаний. Если известны простые вещества, переходите к сложным; от воды до спиртов и эфиров. Зависит от того, нужна тема для классной работы или домашнего обучения; тема изучается впервые или повторяется. Мы подготовили список критериев выбора.
Соответствие ФГОС
Федеральный государственный образовательный стандарт – образец программы обучения, которому следуют школы, вузы, колледжи. Чтобы знания соответствовали экзаменационным критериям, узнайте элементы, прописанные в кодификаторе ФИПИ. Дополнительная литература не гарант заданного школьного образования, но одна из вариативных частей государственной программы.
Стандарт определяется по трём аспектам: программе, условию, результату. Выявить соответствие информации ФГОС легко по печати на издании либо сверив с кодификатором. Гарантировано постепенное продвижение по образовательным ступеням. Дополнительная литература закрепляет и расширяет полученные знания.
Структурированность
12 заданий в ЕГЭ посвящено общей химии, 7 – неорганической, 9 – органической. Из них 4 задания во второй части. Для подготовки берите учебники, которые способны дать теорию к этим заданиям.
На базовом уровне изучают амины, аминокислоты, белки. На профильном представлены нитросоединения, анилин, пептиды, структура белков, пиррол, пиридин, пиримидиновые и пуриновые основания. Отслеживайте наличие этих тем в выбранных учебниках. В структуре они должны подаваться последовательно.
Доступность подачи материала
Наглядность и доступность прослеживаются в компактном способе подачи материала. На определённом этапе можно вернуться к неизученным или непонятным положениям.
Нестандартные задачи формируют изобретательность, творческое мышление, умение упрощать формулы, создавая новые решения. Необычные задания бывают простыми словесными, среднего уровня, олимпиадными. Игровой формат материала мотивирует к углублённому изучению химии, увеличивает удовольствие от получения знаний. Отдавайте предпочтение иллюстрированным, детальным пособиям.
Разнообразие заданий
Химические задания делятся на пять видов: тестовые, расчётные, качественные, экспериментальные, комбинированные. Основные цели задач – составление и решение химических уравнений, демонстрация теории на практике.
Все эти виды есть в школьной программе ФГОС. Задания из дополнительных пособий должны соответствовать системе ГИА.
Лучшие учебники по алгебре
Теория к заданию 11 из ЕГЭ по химии
Классификация органических соединений
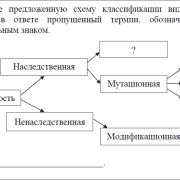
Известно, что свойства органических веществ определяются их составом и химическим строением. Поэтому неудивительно, что в основе классификации органических соединений лежит именно теория строения — теория А. М. Бутлерова. Классифицируют органические вещества по наличию и порядку соединения атомов в их молекулах. Наиболее прочной и малоизменяемой частью молекулы органического вещества является ее скелет — цепь атомов углерода. В зависимости от порядка соединения атомов углерода в этой цепи вещества делятся на ациклические, не содержащие замкнутых цепей атомов углерода в молекулах, и карбоциклические, содержащие такие цепи (циклы) в молекулах.
Классификация органических веществ (по строению углеродной цепи молекул).
Помимо атомов углерода и водорода молекулы органических веществ могут содержать атомы и других химических элементов. Вещества, в молекулах которых эти так называемые гетероатомы включены в замкнутую цепь, относят к гетероциклическим соединениям.
Гетероатомы (кислород, азот и др.) могут входить в состав молекул и ациклических соединений, образуя в них функциональные группы, например, гидроксильную — $ОН$, карбонильную , карбоксильную — , аминогруппу — $NH_2$.
Номенклатура органических соединений
В начале развития органической химии открываемым соединениям присваивались тривиальные названия, часто связанные с историей их получения: уксусная кислота (являющаяся основой винного уксуса), масляная кислота (образующаяся в сливочном масле), гликоль (т.е. сладкий) и т.д. По мере увеличения числа новых открытых веществ возникла необходимость связывать названия с их строением. Так появились рациональные названия: метил амин, диэтиламин, этиловый спирт, метилэтилкетон, в основе которых лежит название простейшего соединения. Для более сложных соединений рациональная номенклатура непригодна.
Теория строения А. М. Бутлерова стала основой для классификации и номенклатуры органических соединений по структурным элементам и по расположению атомов углерода в молекуле. В настоящее время наиболее употребляемой является номенклатура, разработанная Международным союзом теоретической и прикладной химии (IUРАС), которая называется номенклатурой ИЮПАК. Правила ИЮПАК рекомендуют для образования названий несколько принципов, один из них — принцип замещения. На основе этого разработана заместительная номенклатура, которая является наиболее универсальной. Приведем несколько основных правил заместительной номенклатуры и рассмотрим их применение на примере гетерофункционального соединения, содержащего две функциональные группы, — аминокислоты лейцина:
1. В основе названия соединений лежит родоначальная структура (главная цепь ациклической молекулы, карбоциклическая или гетероциклическая система). Название родоначальной структуры составляет основу названия, корень слова.
В данном случае родоначальной структурой является цепь из пяти атомов углерода, связанных одинарными связями. Таким образом, коренная часть названия — пентан.
2. Характеристические группы и заместители (структурные элементы) обозначаются префиксами и суффиксами. Характеристические группы подразделяются по старшинству. Порядок старшинства основных групп:
Выявляют старшую характеристическую группу, которую обозначают в суффиксе. Все остальные заместители называют в префиксе в алфавитном порядке.
В данном случае старшей характеристической группой является карбоксильная, т.е. это соединение относится к классу карбоновых кислот, поэтому к коренной части названия добавляем -овая кислота. Второй по старшинству группой является аминогруппа, которая обозначается префиксом амино-. Кроме этого, молекула содержит углеводородный заместитель метил-. Таким образом, основой названия является аминометилпентановая кислота.
3. В название включают обозначение двойной и тройной связи, которое идет сразу после корня. Рассматриваемое соединение не содержит кратных связей.
4. Атомы родоначальной структуры нумеруют. Нумерацию начинают с того конца углеродной цепи, к которому ближе расположена старшая характеристическая группа:
Нумерацию цепи начинают с атома углерода, входящего в состав карбоксильной группы, ему присваивается номер $1$. В этом случае аминогруппа окажется при углероде $2$, а метил — при углероде $4$.
Таким образом, природная аминокислота лейцин по правилам номенклатуры ИЮПАК называется $2$-амино-$4$-метилпентановая кислота.
Какой учебник по химии лучше
На основе сравнения достоинств, недостатков, актуальности информации, наличия гдз команда ВыборЭксперта.ру выбрала 4 издания для подготовки к экзаменам и углубления знаний по химии:
- Для изучения азов подойдёт учебник 8 класса Габриелян.
- Начала органики кратко и интересно описаны в учебнике 9 класса Рудзитис.
- Если нужен профильный учебник химии, рекомендуем материалы Ерёмина за 11 класс.
- Вдогонку к учебнику возьмите углублённый справочник Ерёмина для отработки и повторения теории.
Основываясь на критериях выбора, наших рекомендациях, составьте личный список литературы. Указанных книг достаточно для освоения общей, неорганической и органической химии на профильном уровне.
Пример 1
Установите соответствие между видом воздействия на равновесную систему и направлением смещения химического равновесия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
CO32- + H2O ⇄ HCO3— + OH— — Q
| ВОЗДЕЙСТВИЕА) добавление кислотыБ) повышение температурыВ) добавление катализатораГ) разбавление раствора | НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ1) в сторону прямой реакции2) в сторону обратной реакции3) практически не смещается |
Решение
А) Добавление кислоты. Видим, что в нашей реакции нет никакой кислоты. Будет ли изменяться равновесие в системе? Конечно, ведь кислота всегда реагирует со щелочью, а за щелочь в реакции отвечают гидроксид-ионы. Равновесие смещается в сторону протекания реакции, то есть вправо.
Б) Повышение температуры смещает равновесие в сторону эндотермической реакции, то есть туда, где теплоты меньше. В сторону прямой реакции.
В) Катализатор не влияет на положение равновесия.
Г) Разбавление раствора – это то же самое, что и добавление воды. А увеличение концентрации реагента смещает равновесие в сторону образования продуктов.
Ответ: 1131.
Если вам все же достанется добавление твердого вещества в качестве воздействия на равновесную систему, помните:
- Твердое нерастворимое вещество не влияет на равновесие.
- Твердое растворимое вещество диссоциирует на ионы. Увеличение концентрации ионов может повлиять на равновесие.
- Твердое растворимое вещество может взаимодействовать с одним из участников реакции. В таком случае равновесие сместится в сторону протекания реакции.
Какие темы есть в ЕГЭ по химии?
Чтобы успешно сдать ЕГЭ по химии 2022, нужно освоить пять разделов этой науки.
Теоретические основы химии
Этот блок включает в себя информацию о строении атомов, об их существовании в молекулах вещества. Выпускникам нужно продемонстрировать навыки работы с таблицей химических элементов Д.И. Менделеева. Этот раздел поможет решить задания 1-4, 17-19, 22 в первой части, а также задание 29 во второй части.
Неорганическая химия
Этой теме посвящены задания 5-9, 20, 21, 23 (первая часть), 30, 31 (вторая часть). Вас ждут любые свойства неорганических соединений: от простых веществ-металлов и неметаллов до комплексных солей и кристаллогидратов. Чтобы получить высокие баллы, необходимо также знать правила номенклатуры, способы получения и основы процессов гидролиза и электролиза.
Органическая химия
В заданиях 10-16 и 32 вы столкнетесь с органической химией. Ученики, которые готовятся самостоятельно, часто стараются выучить все классы веществ по стандартному плану: название класса, номенклатура, физические и химические свойства, способы получения и применение. На самом деле можно значительно облегчить себе жизнь и начать со строения органических молекул. Как только вы поймете, что кратные связи можно разорвать одним набором реактивов, в группе –ОН замещают атом водорода, а –NH2 группа реагирует с кислотами, классы органических веществ и их реакции покажутся однотипными.
Химия и жизнь
Название этого раздела кажется простым и понятным. К сожалению, именно здесь ученики чаще всего теряют баллы. В задании 24 необходимо мысленно представить эксперимент и написать, что произойдет при смешивании заданных веществ. Например, может выпасть осадок, выделиться газ, а может вообще ничего не произойти. В задании 25 нужно определить, где используют то или иное химическое соединение. Ответом может быть химическая промышленность, медицина, сельское хозяйство и, конечно, повседневная жизнь человека.
Решение расчетных задач
Очень важная часть экзамена по химии. В заданиях 26, 27 и 28 в первой части нужно дать ответ в виде числа, не записывая решение. Обычно эти задачи решаются в одно действие — они проверяют не знания химических процессов, а навыки работы с калькулятором.
Задание 33, по мнению многих учеников — самое сложное во всем экзамене. Чтобы его решить, нужно знать химические свойства веществ, уметь составлять причинно-следственные связи в химических системах, понимать, какие вещества реагируют без остатка и почему. Кроме того, в последние годы все чаще встречаются задачи, которые необходимо решать с помощью линейных уравнений или их систем.
В задаче 34 нужно выполнить расчеты, которые позволят установить молекулярную формулу некоторого органического вещества. Далее, используя описание, необходимо представить эту формулу в структурном виде, показывая связи между атомами. Обязательно запишите в ответе уравнение реакции, о которой идет речь в условии!
Пример 2
Установите соответствие между видом воздействия на равновесную систему и направлением смещения химического равновесия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
NH3(г) + H2O(ж) ⇄ NH4+(р-р) + OH—(р-р)
| ВОЗДЕЙСТВИЕА) добавление хлорида калияБ) повышение давленияВ) добавление катализатораГ) добавление твердой щелочи | НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ1) в сторону прямой реакции2) в сторону обратной реакции3) практически не смещается |
Решение
Начнем с уже привычных нам давления и катализатора. Катализатор не влияет на смещение равновесия (ответ 3), а повышение давления смещает равновесие в сторону меньшего количества газов, то есть в сторону прямой реакции (ответ 1).
Теперь обратимся к варианту А. Хлорид калия – растворимое вещество, значит, в растворе будет диссоциировать на ионы калия и хлорид-ионы. Но ни те, ни другие не будут взаимодействовать с нашими участниками реакции. Следовательно, KCl не влияет на равновесие системы.
В варианте Г нам предлагают рассмотреть добавление твердой щелочи. Здесь легко попасть в ловушку, ведь твердые вещества не смещают равновесие. Но не стоит забывать, что любая щелочь – это растворимое основание, а значит, она продиссоциирует в водном растворе на ионы Н+ и ОН—, тем самым увеличивая концентрацию гидроксид-ионов. А при увеличении продуктов реакции равновесие смещается в сторону обратной реакции — ответ 2.
Так мы получили ответ 3132.
Как видите, задание 24 ЕГЭ по химии не стало сложнее! Для его успешного выполнения вам необходимо вспомнить принцип Ле Шателье, а также обратить внимание на растворимость твердых веществ, если они присутствуют. Если хотите разобраться с остальными темами, обязательно приходите к нам на бесплатную консультацию
И удачи в подготовке!
Сдавать ли химию в 2021 году?
Важно! В 2021 году сдавать ЕГЭ по химии и другим предметам на выбор не потребуется выпускникам, которые не будут подавать документы в ВУЗ. Данной категории 11-классиков будет достаточно сдать 2 основных предмета — русский язык и математику
Если ситуация с коронавирусом стабилизируется, ГИА-2021 года пройдет в штатном формате. Это значит, что выпускников ждет три сессии ЕГЭ:
- досрочная (конец марта – начало апреля) — отменена!;
- основная (май – июнь);
- осенние пересдачи (сентябрь).
Сдать ЕГЭ по химии в рамках ГИА 2021 года можно будет только в ходе первых двух сессии. В сентябре предполагается пересдача только обязательных дисциплин – русского языка и математики.
В 2020 году химию, как один из предметов по выбору, сдавали менее 15% участников Единого Государственного Экзамена (около 60 439 человек). Но, в министерстве ожидают, что в 2021 году химия будет более популярна среди выпускников, ведь именно этот сертификат является необходимым условием для вступления в медицинские университеты России. Также высокие баллы по данному предмету могут открыть будущему абитуриенту двери в таких направлениях, как:
- биотехнологии (19.03.01);
- биохимия (03.01.03);
- медицинская биохимия (30.05.01);
- химическая технология (18.03.01);
- фармация (33.05.01);
- архитектура живых систем (19.03.01);
- учитель химии (05.01.01).
Обратите внимание, что в некоторых ВУЗах помимо сертификата по химии, могут потребовать результат ЕГЭ по биологии
Бесплатно
CHEMEGE.RU
Сайт: https://chemege.ru
На сайте вы найдете полный теоретический курс подготовки к ЕГЭ по химии-2021. Приведена теория по каждому заданию в соответствии с кодификатором.
К части тем есть тренировочные тесты и задачи. Также есть раздел с видеоопытами по общей, неорганической и органической химии.
ЕГЭ.рф
Сайт: https://егэ.рф
Сайт предоставляет шанс всем желающим пройти ЕГЭ по химии для оценки текущего уровня подготовки. Тестирование проводится онлайн на реальных вариантах ЕГЭ. Платформа сотрудничает с ФИПИ.
Тестовую часть проверяет компьютер, результат будет доступен сразу. Письменную часть можно отправить на проверку реальному эксперту ЕГЭ. Стоимость услуги: 500 р. — оценка письменной части без комментариев, 1000 р. — с развернутыми комментариями эксперта.
«4ЕГЭ»
Сайт: https://4ege.ru
Здесь вы найдете материалы для подготовки к ЕГЭ по химии по разным темам:
- Видеоразборы отдельных заданий в ЕГЭ по химии
- Методические пособия с теорией
- Записи вебинаров по теоретическим темам
- Шпаргалки для запоминания
«Синергия»
Сайт: https://synergy.ru
На сайте собраны все актуальные материалы по теме ЕГЭ по химии:
- Демоверсии и КИМы за 2021 год
- ЕГЭ предыдущих периодов (2019-2020)
- Теоретическая часть: по каждому типу заданий ЕГЭ, а также химия в схемах и таблицах, таблица Менделеева, таблица растворимости
- Практическая часть: подборка задач по каждому типу заданий ЕГЭ с ответами для самопроверки
«РешуЕГЭ»
Сайт: https://chem-ege.sdamgia.ru
Это сайт-тренажер, где каждый месяц появляются новые варианты тренировочных заданий по химии: тестовой части и с развернутым ответом. Варианты генерируются компьютером: из новых заданий и самых сложных заданий по статистике прошлого месяца.
Чтобы проверить свои знания по определенному разделу химии, можно сформировать тест самостоятельно — из каталога заданий по интересующим вас темам.
Яндекс.Репетитор
Сайт: https://yandex.ru
Здесь вы найдете 6 видео-уроков по 45 минут по темам:
- Решение расчетных задач
- Классификация неорганических веществ. Химические свойства основных классов неорганических веществ
- Окислительно-восстановительные реакции. Электролиз
- Химические реакции. Скорость химической реакции. Химическое равновесие
- Строение вещества
- Строение атома. Периодический закон
Также здесь можно порешать тесты. Варианты похожи на те, что используются на реальном ЕГЭ, потому что их составляют эксперты, в том числе авторы «СтатГрада». Каталог заданий регулярно обновляется.
«Птичка Химичка -Химия с Нуля-«
Сайт: https://www.youtube.com
Автор канала обещает помочь всем желающим разобраться в химии.
Здесь собраны видео по разным темам:
- Что нужно знать для ЕГЭ
- Актуальная информация по ЕГЭ 2021
- Полный курс химии из 92 уроков
- 71 видео по теме: Общая химия. Понятия. Законы. Формулы
- Видео по отдельным темам: Органическая химия, Типы химических связей, Классы неорганических соединений, Неорганическая химия
Смотреть видео нужно подряд, не пропуская уроков, и результат не заставит себя ждать.
«examtop»
Сайт: https://www.youtube.com
На канале выходят видеоуроки для подготовки к ЕГЭ по химии с доп. материалами и актуальными заданиями 2021 года.
В плейлистах собраны уроки по темам:
- Курс: Задание 34 ЕГЭ по химии (на примерах реальных задач). 69 видео
- Курс: Органическая химия. Подготовка к ЕГЭ. 20 видео
- Курс: Неорганическая химия. Подготовка к ЕГЭ. 17 видео
- Видео-разборы отдельных заданий ЕГЭ по химии
«Химия ЕГЭ 2021 — АКАДЕМИЯ ЕГЭ N1»
Сайт: https://www.youtube.com
В бесплатном доступе 129+ видеоуроков с разборами заданий из ЕГЭ по химии и теорией к экзамену. В отдельном плейлисте собраны прямые трансляции с разбором заданий, полезными фишками и лайфхаками по подготовке. Новые уроки выходят 2 раза в неделю.
Общая информация
Реформа системы контроля качества знаний завершена и в 2021 году ФИПИ не планирует какие-либо изменения для ЕГЭ по химии. Формат и содержание экзамена будут максимально приближены к прошлогодним. Лишь в некоторых отдельных заданиях, которые вызовут больше всего нареканий со стороны 11-классников и учителей, могут быть мелкие доработки.
На данный момент можно с уверенностью говорить о таких основополагающих фактах для ЕГЭ по химии 2021 года:
- экзамен будет проведен во всех регионах России в единый день (по календарю ГИА-2021);
- в КИМе всего 35 заданий;
- на выполнение работы отведено 3,5 часа (210 минут);
- разрешено использование непрограммируемого калькулятора и трех таблиц (предоставляются организаторами);
- максимальный ПБ (первичный балл) – 60;
- необходимый минимум – 36 ТБ (тестовых баллов) или же 13 ПБ (первичных баллов).
Виртуальные лаборатории
Российский портал, на котором эксперименты из школьной программы можно смоделировать онлайн.
Международный ресурс, которые разрабатывают учёные со всего мира. Позволяет ставить более серьёзные опыты.
Проект по доставке на дом наборов для экспериментов. Также на сайте есть подробные и корректные инструкции по выполнению опытов. Многие ингредиенты для этих опытов можно самостоятельно купить в аптеке или продовольственном магазине. В дополнение к опытам на Mel Science полезно смотреть видео, которые объясняют суть химических явлений.

На портале есть множество полезных статей, подробные разборы опытов, инструкции, как проводить их в домашних условиях и где брать для них реактивы.
Теория к заданию 10 из ЕГЭ по химии
Взаимосвязь различных классов неорганических веществ
Материальный мир, в котором мы живем и крохотной частичкой которого мы являемся, един и в то же время бесконечно разнообразен. Единство и многообразие химических веществ этого мира наиболее ярко проявляется в генетической связи веществ, которая отражается в так называемых генетических рядах. Выделим наиболее характерные признаки таких рядов:
1. Все вещества этого ряда должны быть образованы одним химическим элементом. Например, ряд, записанный с помощью следующих формул:
$Br_2 → HBr → NaBr → NaNO_3$,
нельзя считать генетическим, т.к. в последнем звене элемент бром отсутствует, хотя реакция для перехода от $NaBr$ к $NaNO_3$ легко осуществима:
$NaBr + AgNO_3 = AgBr↓+ NaNO_3$.
Этот ряд мог бы считаться генетическим рядом элемента брома, если бы его завершили, например, так:
$Br_2 → HBr → NaBr → AgBr$.
2. Вещества, образованные одним и тем же элементом, должны принадлежать к различным классам, т.е. отражать разные формы его существования.
3. Вещества, образующие генетический ряд одного элемента, должны быть связаны взаимопревращениями. По этому признаку можно различать полные и неполные генетические ряды.
Например, приведенный выше генетический ряд брома будет неполным, незавершенным. А вот следующий ряд:
$Br_2 → HBr → NaBr → AgBr → Br_2$
уже можно рассматривать как полный: он начинался простым веществом — бромом и им же закончился. Обобщая сказанное выше, можно дать следующее определение генетического ряда.
Генетическим называется ряд веществ — представителей разных классов, являющихся соединениями одного химического элемента, связанных взаимопревращениями и отражающих общность происхождения этих веществ или их генезис.
Генетическая связь — понятие более общее, чем генетический ряд, который является пусть и ярким, но частным проявлением этой связи, реализующейся при любых взаимных превращениях веществ. Тогда, очевидно, под это определение подходит и первый приведенный в тексте ряд веществ.
Для характеристики генетической связи неорганических веществ мы рассмотрим три разновидности генетических рядов.
Генетический ряд металла.
Наиболее богат ряд металла, у которого проявляются разные степени окисления. В качестве примера рассмотрим генетический ряд железа со степенями окисления $+2$ и $+3$:
${Fe}{\text»металл»}→{FeCl_2}{\text»соль — хлорид железа(II)»}$ $→{Fe(OH)_2}{\text»основание — гидроксид железа(II)»}$ $→{FeO}{\text»основный оксид — оксид железа(II)»}$ $→{Fe}{\text»металл»}$ $→{FeCl_3}{\text»соль — хлорид железа(III)»}$ $→{Fe(OH)_3}{\text»гидроксид железа (III) — амфотерное соединение с преобладанием основных свойств»}$ $→{Fe_2O_3}{\text»оксид железа(III), аналогичен по свойствам соответствующему гидроксиду»}$ $→{Fe}{\text»металл»}$
Напомним, что для окисления железа в хлорид железа (II) нужно взять более слабый окислитель, чем для получения хлорида железа (III):
Генетический ряд неметалла.
Аналогично ряду металла более богат связями ряд неметалла с разными степенями окисления, например, генетический ряд серы со степенями окисления $+4$ и $+6$:
${S}{\text»неметалл»} → {SO_2}{\text»кислотный оксид — оксид серы (IV)»}$ $ → {H_SO_3}{\text»сернистая кислота»}$ $ → {Na_SO_3}{\text»соль — сульфит натрия»}$ $ → {SO_2}{\text»кислотный оксид — оксид серы (IV)»}$ $ → {SO_3}{\text»кислотный оксид — оксид серы (VI)»} $ $ → {H_SO_4}{\text»серная кислота»}$ $ → {SO_2}{\text»кислотный оксид — оксид серы (IV)»} $ $→ {S}{\text»неметалл»}$
Затруднение может вызвать лишь последний переход. Руководствуйтесь правилом: чтобы получить простое вещество из окисленного соединения элемента, нужно взять для этой цели самое восстановленное его соединение, например, летучее водородное соединение неметалла. В нашем случае:
${SO_2}{+4}+2H_2{S}{-2}=2H_2O+S{0}↓.$
По этой реакции в природе из вулканических газов образуется сера.
Аналогично для хлора:
Генетический ряд металла, которому соответствуют амфотерные оксид и гидроксид, очень богат связями, т.к. они проявляют в зависимости от условий то кислотные, то основные свойства.
Например, рассмотрим генетический ряд цинка:
Что такое равновесие?
Чтобы решить 24 задание ЕГЭ по химии, для начала вспомним, что такое равновесие и как его смещать.
Химическое равновесие — состояние химической системы, при котором скорость прямой реакции равна скорости обратной.
Записав уравнение химической реакции в тетради, мы можем понять, какое количество реагентов вступает в эту реакцию, какие продукты мы получаем. Но на практике превращения далеки от идеала. Вещества реагируют не полностью, образуются отходы, возникают потери. Смещение равновесия позволяет регулировать течение реакции так, как этого требует производственный процесс.
Мы будем сталкиваться с понятиями «смещение в сторону прямой реакции» или «в сторону продуктов». Это означает, что в результате реакции мы сможем получить больше продуктов, то есть увеличить выход.
«Смещение в сторону обратной реакции» или «в сторону реагентов» позволяет уменьшить выход продуктов, уменьшить их выход и тем самым увеличить выход обратной реакции.
В 1884 году французский химик Анри Ле Шателье сформулировал принцип, согласно которому, при воздействии на систему, находящуюся в состоянии равновесия (температура, давление, концентрация), система стремится компенсировать внешнее воздействие.
- При увеличении давления равновесие смещается в сторону меньших газов, при уменьшении давления — в сторону больших газов;
- При увеличении температуры равновесие смещается в сторону эндотермической реакции, при уменьшении — в сторону экзотермической реакции;
- При увеличении концентрации реагентов равновесие смещается в сторону продуктов реакции и наоборот.
Посмотрим, как в 2020 году изменили варианты ответов, сделав это задание «суперсложным» (на самом деле нет).
Самостоятельно подготовиться к ЕГЭ непросто. На то, чтобы разобраться со всеми темами, понадобится много времени. Но и это не решит проблему! Например, если вы запомнили какое-то решение из интернета, а оно оказалось неправильным, можно на пустом месте потерять баллы
Если хотите научиться решать все задания ЕГЭ по химии, обратите внимание на онлайн-курсы MAXIMUM! Наши специалисты уже проанализировали сотни вариантов ЕГЭ и подготовили для вас вас максимально полезные занятия.Приходите к нам на консультацию — вы сможете пройти диагностику по выбранным предметам ЕГЭ, поставить цели и составить стратегию подготовки, чтобы получить на экзамене высокие баллы. Все это абсолютно бесплатно!
Рейтинг учебников по химии
Наши эксперты выяснили, какое пособие по дисциплине педагоги считают лучшим. При составлении рейтинга учитывались следующие параметры: последовательность тем; понятность определений; наличие разноуровневых заданий для подготовки к ЕГЭ. Каждый из учебников имеет свои особенности.
К критериям отбора качественных пособий относятся:
- Структурированность текста;
- Разнообразие заданий;
- Соответствие ФГОС;
- Качество печати;
- Год издания.
Кроме указанных параметров, мы учли опыт авторов-составителей и дизайн разделов. Интерактивные формы со схемами, знаками, таблицами способствуют качественному усвоению материала.